









 Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.
Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.

Indikace k provedení HPV testu by měla sledovat jasně dané klinické situace. V těchto případech jeho výsledek zásadním způsobem zpřesňuje stanovení míry rizika aktuální přítomnosti závažné prekancerózy děložního hrdla. Mimoto navíc poskytuje významnou prediktivní hodnotu ohledně pravděpodobnosti výskytu cervikální dysplázie v horizontu příštích let. Tyto informace vedou jak k optimalizaci screeningového programu, tak k individualizaci sledování rizikových žen a redukci počtu prováděných zákroků na děložním hrdle. Naproti tomu chybně indikovaný HPV test nejenže nepřináší další informaci o závažnosti přednádorového stavu, ale vyvolá u pacientky obavy z nejasného výsledku, vede ke kumulaci dalších vyšetření a konzultací a ve výsledku může dospět až k chybně indikované konizaci. Účelem tohoto přehledového článku je sumarizovat indikace k provedení HPV testu a poskytnout průvodce stran stanovení dalšího léčebného managementu v závislosti na jeho výsledku a konkrétní klinické situaci.
Lidský papilomavirus (HPV) je původcem naprosté většiny cervikálních karcinomů. Přestože se s tímto virem během života setká většina žen, přednádorová či nádorová léze se vyvine pouze u zlomku z nich. Samotný průkaz přítomnosti tohoto viru proto automaticky neznamená jistotu rozvoje dysplázie nebo karcinomu. Nejvýznamnější rizikový faktor spojený se vznikem cervikálního karcinomu představuje až dlouhodobá perzistence HPV infekce. S potenciálem maligní transformace jsou spojeny pouze vybrané genotypy označované jako onkogenní, „high-risk“ (16, 18, 45, 31, 33 a další). Naopak stanovení neonkogenních, „low-risk“ genotypů nemá žádný klinický přínos.
HPV testem je myšlen průkaz 13-14 onkogenních genotypů a v klinické praxi je indikován zejména v následujících situacích: 1) primární HPV screening, který je v současnosti implementován v celé řadě západních zemí; 2) třídění (triage) některých abnormálních cytologických výsledků; 3) sledování pacientek po zákroku (většinou konizaci) provedeném pro přednádorovou lézi nebo časný karcinom.
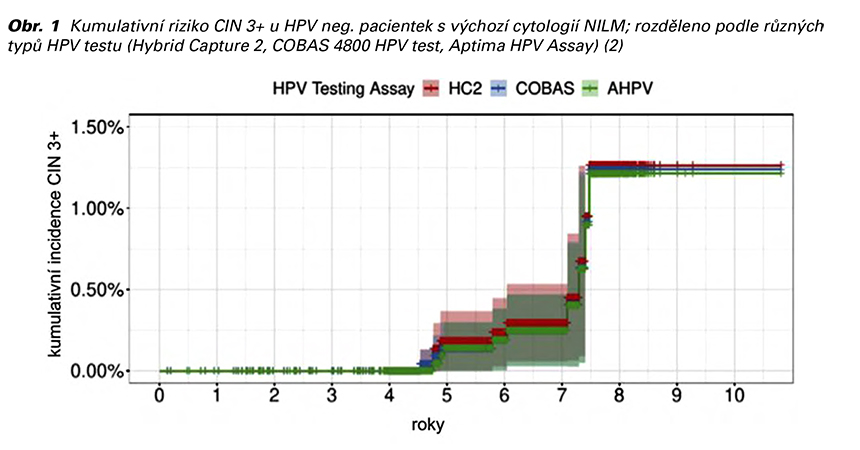
Kombinace negativního HPV testu a negativní cytologie poskytuje téměř jistotu, že na děložním hrdle není aktuálně přítomna závažná prekanceróza či karcinom. Podle dat ze sítě nemocnic Kaiser Permanente v severní Kalifornii, které jsou podkladem pro americké doporučené postupy, je riziko přítomnosti CIN3 v této klinické situaci 0,001 % a CIN2 0,08 % (1). Z longitudinálních studií je dále patrné, že riziko rozvoje závažné prekancerózy je i do budoucna mimořádně nízké (viz Obr. 1). V současnosti jsou k dispozici data z desetiletého sledování (studie FOCAL-DECADE), ze kterých vyplývá, že je zmiňované riziko i v tomto časovém horizontu hluboko pod 2 % (2). Do pěti let je navíc riziko při vstupní HPV negativitě téměř nulové. Tomuto je v řadě zemí přizpůsoben interval screeningových kontrol, které mohou být v případě negativního výsledku prodlouženy až na 5 let.
Riziko aktuální přítomnosti CIN3 se v tomto případě pohybuje okolo 2 % a je výrazně závislé na konkrétním genotypu HPV. V případě přítomnosti HPV 16 je riziko 5%, u pozitivity HPV 18 je 3% a u pozitivity HPV 31, 33, 52 a 58 je 2%. U ostatních genotypů nepřesahuje aktuální riziko 1 % (1). HPV genotypizace tedy představuje účinný nástroj k třídění HPV pozitivních pacientek s negativní cytologií. HPV 16 či 18 pozitivní pacientky by měly být referovány přímo k expertní kolposkopii. Ostatním pacientkám je možné nabídnout opakování cytologie za 6 měsíců nebo provedení testu využívajícího duálního imunocytochemického barvení stanovujícího proteiny p16/Ki-67 (CINtec Plus, Roche lab.). Cytologie je zatížená limitovanou senzitivitou pohybující se okolo 50-60 %. V rámci primárního screeningu je tento nedostatek eliminován opakovaným odběrem za 1 rok. Naproti tomu v rámci sledování rizikových HPV pozitivních pacientek představuje nízká senzitivita, výrazná inter a intra-observační variabilita a limitovaná schopnost detekovat adenoléze významnou překážku. Oproti tomu vykazuje duální imunocytochemický test senzitivitu výrazně vyšší, a je proto v této situaci vhodnější (3). Další výhodou duálního barvení je jednoznačnost výsledku (pozitivní/negativní). Není proto potřeba speciální doporučení pro jeho interpretaci. V případě HPV non 16/18 pozitivity, negativní cytologie a negativního výsledku testu CINtec Plus je možné provést další cytologické vyšetření až za rok. Randomizovaná, prospektivní studie NCI/KPNC doložila dokonce 3letý bezpečný interval ke kontrole v případě doložení negativity duálního barvení (4). Pozitivní CINtec Plus v této situaci naopak implikuje referování pacientky ke kolposkopické expertíze.
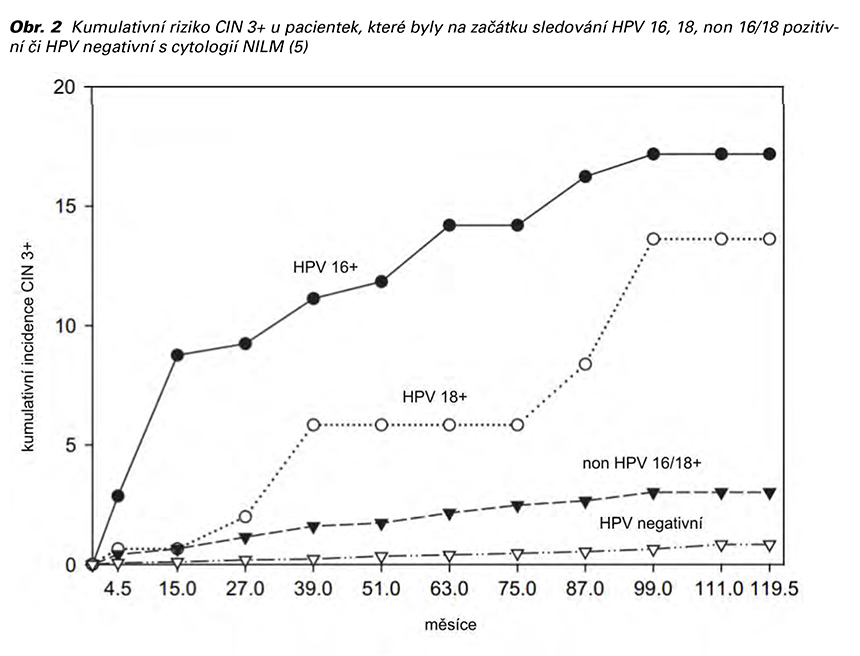
V případě negativity duálního barvení nebo kolposkopického vyšetření u referovaných pacientek je možné zvolit vyčkávací strategii. Důvodem je vysoký podíl spontánní eliminace HPV infekce bez ohledu na věk pacientek. V české studii Libuše, která zkoumala vývoj HPV infekce v kohortě žen starších třiceti let, došlo v rámci tříletého sledování u 43 % pacientek ke spontánní regresi. Medián věku těchto žen činil 41 let. Naproti tomu u 51 % žen HPV infekce perzistovala. Spontánní vymizení HPV infekce se tedy týká i žen nad 40 let (5). HPV perzistence je jednoznačným rizikovým faktorem pro vznik závažné prekancerózy v budoucnosti. Tato skutečnost je výrazně více vyjádřena u HPV 16 a 18 než u ostatních genotypů (viz Obr. 2) (6). Jedná se o další důvod, proč by HPV 16 či 18 pozitivní pacientky měly být sledovány v ambulanci expertní kolposkopie.
HPV test může být využit za účelem stratifikace rizika spojeného s vybranými kategoriemi abnormální cytologie. Již přes 20 let jsou známy výsledky studie ALTS (ASCUS/LSIL Triage Study), která potvrdila třídící schopnost HPV testu v případě kategorie ASC -US. Naproti tomu u pacientek s cytologií LSIL není provedení HPV testu přínosem pro jeho nízkou specifitu (příliš mnoho žen s cytologií LSIL je HPV pozitivních) (7). Specifita HPV testu však výrazně narůstá s přibývajícím věkem. Z toho vyplývá, že i v rámci kategorie LSIL je možné HPV test použít u menopauzálních žen k selekci kohorty (HPV negativních), u kterých nebude nutné indikovat konizaci. Mnohem výhodněji lze ale u žen s cytologií LSIL uplatnit duální imunocytochemický test CINtec Plus. Jeho specifita je v této klinické situaci významně vyšší než specifita HPV testu (8). HPV test je možné využít k třídění (zejména starších) pacientek s cytologií ASC-H a negativní nebo neadekvátní kolposkopií či opakovaným nálezem AGC-NOS. Naproti tomu tento test nepřináší žádnou další informaci v kombinaci s cytologií HSIL - tyto ženy by měly být rovnou referovány k expertní kolposkopii. Rovněž u pacientek pod 30 let je HPV test zatížen nízkou specificitou (velká část mladých HPV pozitivních pacientek se viru sama zbaví, aniž by byla infekce spojena s rizikem rozvoje dysplázie).
HPV test je klíčovým vyšetřením, které by mělo být provedeno v rámci sledování pacientek, u kterých bylo děložní hrdlo chirurgicky ošetřeno pro prekancerózu či časný karcinom. Základním cílem provedení konizace je vedle fyzického odstranění dysplázie i eliminace HPV infekce. Operace na děložním hrdle aktivuje lokální imunitní reakci, která eliminuje případná reziduální ložiska infekce. Je proto vhodné neprovádět HPV test dříve než za půl roku po konizaci (někteří autoři doporučují až interval jednoho roku). Perzistence HPV infekce i po tomto intervalu je zásadním rizikovým faktorem pro výskyt recidivy dysplázie, zejména pak v situaci, kdy je patrna konkordance s původním genotypem, který byl příčinou ošetřené léze.
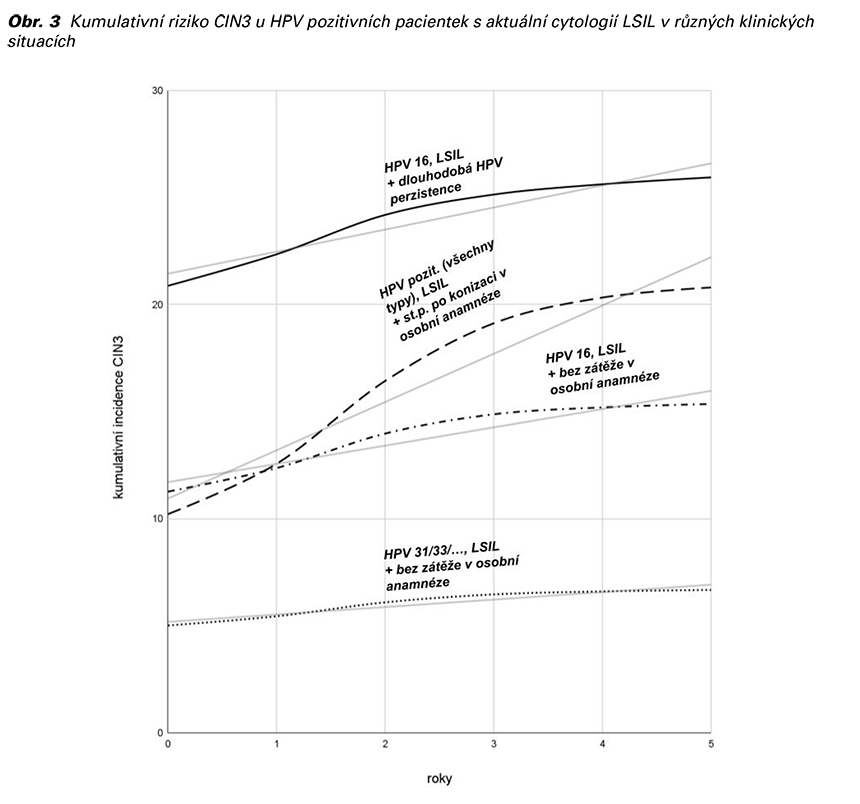
V klinické praxi se často lze setkat s HPV pozitivními pacientkami, které v minulosti prodělaly ošetření závažné prekancerózy. Na tyto pacientky je nutno pohlížet jako na vysoce rizikové. Kumulativní nárůst rizika rozvoje závažné prekancerózy je výrazně vyšší v porovnání s HPV pozitivními pacientkami bez osobní anamnézy zatížené prodělaným ošetřením závažné prekancerózy. Obrázek 3 ilustruje kumulativní riziko výskytu CIN3 u HPV pozitivních pacientek s cytologií LSIL v jednotlivých diskutovaných klinických situacích (1).
HPV test poskytuje unikátní možnost stanovení původce téměř všech karcinomů děložního hrdla. Je možné jej použít u širokého spektra pacientek - od zdravých žen v rámci screeningu, až ke sledování pacientek s ukončenou léčbou karcinomu. Narozdíl od cytologie, která přeneseně poskytuje informaci o možné aktuální přítomnosti dysplázie, přináší HPV test i významnou a dlouhodobou prediktivní hodnotu. Zapojení HPV testu do každodenní klinické praxe proto umožní omezit počet potřebných kontrol a jejich zacílení na pacientky, které jsou opravdu ohroženy rizikem rozvoje karcinomu děložního hrdla.