









 Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.
Rada pro výzkum, vývoj a inovace: Seznam recenzovaných neimpaktovaných časopisů vydávaných v ČR
Oficielní časopis České společnosti pro ultrazvuk v porodnictví a gynekologii.

Endometrióza je chronické recidivujúce ochorenie, ktoré má negatívny vplyv na kvalitu života a fertilitu ženy. Aj napriek tomu, že je endometrióza známa desaťročia, stále neexistuje jasná teória jej vzniku a nepozná sa spoľahlivá neinvazívna metóda, ktorá vie toto ochorenie detekovať. V poslednej dobe pribúdajú dôkazy o tom, že kvalita mikrobiómu ženy môže mať zásadný vplyv na vznik a progresiu endometriózy. Cieľom tohto prehľadového článku je priniesť ucelený prehľad aktuálnych dostupných literárnych zdrojov o možnom vplyve mikrobiómu na vznik a progresiu endometriózy. Informácie boli získané pomocou vybraných kľúčových slov prostredníctvom databázy PubMed.
Endometrióza je chronické recidivujúce ochorenie, ktoré výrazne znižuje kvalitu života ženy. Aj napriek tomu, že je známa už dlho, stále predstavuje v ambulancii gynekológa problém. Toto ochorenie sa v posledných rokoch vyskytuje čoraz častejšie, nezriedka už vo veľmi skorom veku. Úzko súvisí s fertilitou ženy a je častou príčinou neplodnosti. Stále nie je objasnená príčina jej vzniku aj napriek doteraz dostupným teóriám. Taktiež aj napriek mnohým výskumom nie je možné neinvazívne diagnostikovať toto ochorenie. Cieľom nových vedeckých štúdií je dokázať skutočnú príčinu jej vzniku a progresie, čo by zároveň umožnilo lepšie pochopiť problematiku endometriózy, vytvoriť prevenciu tohto ochorenia a navrhnúť účinnú liečbu. Jej odhalenie v skorých štádiách prostredníctvom neinvazívnej diagnostiky by viedlo k včasnej liečbe, znížilo by množstvo komplikácií, ktoré ochorenie v jeho progresii prináša. Prehľadové práce z rokov 2020-2021 zahrňujú štúdie, ktoré potvrdili súvislosti medzi bakteriálnym črevným mikrobiómom a endometriózou (1).
Endometrióza je definovaná ako prítomnosť tkaniva podobného endometriu mimo dutinu maternice, ktoré indukuje chronickú zápalovú reakciu. Najčastejšie je lokalizované v panve, na vaječníkoch, vajcovodoch, peritoneu, črevách a močovom mechúre, zriedkavo aj na vzdialenejších orgánoch v prípade extragenitálnej formy. Je dependentná na estrogénoch a obvykle postihuje ženy v reprodukčnom veku. Tkanivové depozity vytvárajú lokálnu zápalovú reakciu, ktorá pri chronickom pôsobení spôsobuje fibrotické zmeny. Ložiská endometriózy môžu podliehať cyklickým zmenám ako eutopické endometrium, čiže v nich prebieha proliferácia, rozpad a krvácanie (2).
Presná prevalencia endometriózy nie je známa. Odhady sa vo všeobecnej populácii žien pohybujú od 2 % do 10 %. Vyskytuje sa v 20-50 % u neplodných žien a až v 80 % u žien s chronickou panvovou bolesťou. Prítomnosť endometriózy bola zistená počas laparoskopie u 20-50 % bezpríznakových žien. Dedičné predpoklady desaťnásobne zvyšujú riziko u žien, ktoré majú príbuznú v priamej línii postihnutú endometriózou (3).
Symptomatológia endometriózy závisí predovšetkým od jej lokalizácie. Intenzita príznakov však často nekoreluje so stupňom ochorenia. Medzi najčastejšie symptómy endometriózy patrí cyklická panvová bolesť, dyspareunia, bolestivá defekácia a pri progredujúcom ochorení trvalá panvová bolesť so vznikom zrastov v brušnej dutine. Zlatým štandardom diagnostiky ochorenia je laparoskopia. Liečba endometriózy je medikamentózna, chirurgická alebo kombinovaná – medikamentózno – chirurgická (4).
Najstaršia a široko uznávaná hypotéza je implantačná teória retrográdneho krvácania menštruačnej krvi s obsahom fragmentov endometria cez vajíčkovody do peritoneálnej dutiny a následná adhézia a invázia jej zložiek do peritoneálneho mezotelu s vytváraním nových ciev, ktoré umožňujú prežívanie a rast implantovaných ložísk. U asi 1/3 žien s endometriózou sa potvrdili ložiská endometriózy v lymfatických uzlinách, čo podporuje teóriu lymfatického šírenia ochorenia. Vysvetľuje to aj prítomnosť ložísk na vzdialených miestach, ktoré spolu nesusedia. Teória metaplázie coelomu hovorí, že z embryonálneho coelomového epitelu sa diferencuje nielen tkanivo Müllerovho vývodu, teda endometrium, ale aj epitel peritonea, pleurálnej dutiny a bunky zárodočnej vrstvy na povrchu ovária. Imunologická teória zas hovorí, že všetky stavy spojené s imunogenetickou poruchou môžu zvyšovať náchylnosť k vzniku endometriózy. U pacientok s endometriózou sa často vyskytujú poruchy imunity, buď ako následok ochorenia, alebo ako príčina jeho vývoja. Indukčná teória predpokladá, že niektoré hormonálne alebo biologické faktory môžu indukovať diferenciáciu nediferencovaných pluripotentných buniek na endometriálne tkanivo. Tieto látky môžu byť exogénnej, ale aj endogénnej povahy. Teória iatrogénnej diseminácie vysvetľuje prítomnosť endometriózy prednej brušnej steny u pacientok v anamnéze po cisárskom reze či možné šírenie pri opakovaných inštrumentálnych revíziách dutiny maternice. Keďže sa u priamych príbuzných postihnutých žien vyskytuje endometrióza 7x častejšie ako v bežnej populácii, vyvinula sa genetická teória. Teória kmeňových buniek hovorí o diferenciácii mezenchymálnych kmeňových buniek kostnej drene na endometriálne tkanivo. Túto teóriu podporuje štúdia, v ktorej bola popísaná po transplantácii kostnej drene prítomnosť endometria darkyne v endometriu príjemkyne (3). Je dokázané, že endometrium v svojej eutopickej lokalizácii sa u pacientok s endometriózou signifikantne líši od endometria zdravých pacientok. Eutopické endometriálne kmeňové bunky pri endometrióze disponujú vyšším proliferačným potenciálom a exprimujú vo väčšej miere gény potrebné pre inváziu do mezotelu. Otázkou však ostáva to, či epitelový a stromálny komponent endometriálneho ložiska pochádza z jedného klonu kmeňovej bunky alebo sa jedná o klony od seba nezávislých kmeňových buniek. Kmeňové bunky majú perspektívu aj z hľadiska diagnostiky, či cielenej terapie endometriózy (5).
Najnovšie poznatky sa prikláňajú k teórii bakteriálnej kontaminácie a aktivácie imunitného systému. Vznik endometriózy môže byť spôsobený prítomnosťou patogénnych baktérií v maternici, ktoré po čase spúšťajú zápalovú reakciu (3). Na podporu tejto teórie boli nájdené vyššie koncentrácie baktérie E. coli v menštruačnej krvi žien s endometriózou, čo naznačuje, že zvýšené koncentrácie endotoxínu v peritoneálnej tekutine môžu prostredníctvom zápalových molekúl podporovať vznik a progresiu endometriózy (4).
Teória retrográdnej menštruácie hovorí o vycestovaní tkaniva maternice do peritoneálnej dutiny, avšak nevysvetľuje, prečo sa u niektorých žien z daného tkaniva vyvinie endometrióza a u niektorých nie. Čiastočné vysvetlenie daného faktu spočíva v imunitnej dysregulácii u žien s endometriózou, ktorá ovplyvňuje imunitnú odpoveď na prítomnosť tkaniva v peritoneálnej dutine. Ukázalo sa, že pri tomto procese je práve črevný mikrobióm zodpovedný za imunitnú odpoveď. Dysbióza čreva lokálne aktivuje neutrofily ako zápalové bunky, taktiež ničí ochrannú bariéru čreva, čo spôsobuje prienik patogénnych metabolitov do organizmu a následný rozvoj zápalu (6). Výsledkom tohto procesu je zvýšené množstvo makrofágov v peritoneálnej dutine, no ich kapacita fagocytovať implantované lézie endometria je znížená, čo podporuje prežitie a ďalší rast endometriálneho tkaniva. Dysmikróbia čreva môže narušiť imunitné reakcie v peritoneálnej dutine a viesť tak k vzniku a progresii endometriózy (7).
Ľudský mikrobióm zahŕňajúci všetky mikroorganizmy žijúce na tele a v tele človeka má obrovský vplyv na celkový stav organizmu. Dysbióza je definovaná ako nerovnováha alebo poškodenie mikrobiómu. Je spôsobená premnožením patologických mikroorganizmov, či zníženým množstvom probiotických baktérií. Kombinácia týchto faktorov má pozoruhodné dôsledky na ľudské zdravie, je asociovaná napríklad so zápalovými ochoreniami čriev, psoriázou, artritídou alebo rakovinou (8).
Črevný mikrobióm je pravdepodobne jedným z najbohatších a najštudovanejších mikrobiómov. Zistilo sa, že ovplyvňuje metabolizmus estrogénu a homeostázu kmeňových buniek. Metabolity mikróbov, ktoré hosťujú v určitom prostredí menia lokálne mikroprostredie, jeho pH alebo vedú k vzniku ROS (angl. Reactive Oxygen Species). Dôsledkom týchto zložitých interakcií vznikajú niektoré ochorenia ženského reprodukčného traktu ako napr. endometrióza (Obr. 1 a 2) (9,10).
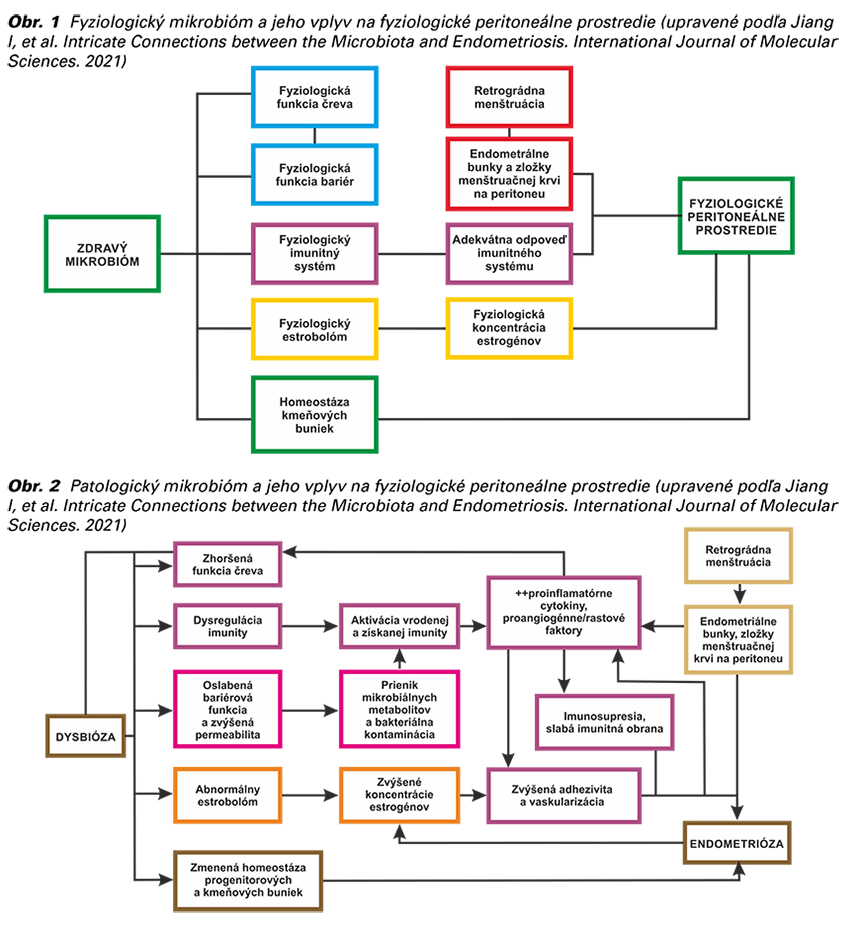
Moreno et al. skúmali zloženie mikrobiómu pošvy a maternice žien. Po analýze boli určené dva druhy mikrobiómov – Lactobacillus dominantné (viac ako 90 % Lactobacillus spp.) a Lactobacillus nedominantné (menej ako 90 % Lactobacillus spp., viac ako 10 % iných baktérií). Okrem toho bolo zistené, že pri Lactobacillus nedominantnom mikrobióme sa u žien vyskytovali reprodukčné problémy. Dominantná prítomnosť Lactobacillus spp. vo vaginálnom prostredí znižuje lokálne pH tým, že produkuje kyselinu mliečnu a mastné kyseliny s krátkym reťazcom, ktoré zabraňujú rastu patogénnych baktérií. Prítomnosť Lactobacillus nedominantného mikrobiómu môže vyvolať v maternici lokálnu zápalovú reakciu. Charakteristickým hlavným znakom pri vzniku a progresii endometriózy je lokálny zápal endometria. Preto je na mieste domnievať sa, že zmenená endometriálna mikroflóra môže súvisieť so vznikom endometriózy (11).
Niekoľko doteraz publikovaných štúdií analyzovalo charakteristiku endometriálneho mikrobiómu zdravých žien v porovnaní so ženami, ktoré trpeli endometriózou. Zistili, že mikrobióm zdravých a asymptomatických žien je vo veľkej miere osídlený rodmi Firmicutes, Bacterioidetes, Proteobacteria a Actinobacteria (4). Moreno et al. identifikovali päť najčastejšie sa vyskytujúcich baktérií u žien v reprodukčnom veku – Lactobacillus, Gardnerella, Bifidobacterium, Streptococcus a Prevotella. Ďalšia štúdia odhalila v endometriálnom mikrobióme dominantné zastúpenie Lactobacillus spp., Mycoplasma hominis, Gardnerella vaginalis a Enterobacter spp. (11).
V poslednom čase pribúda čoraz viac štúdií, ktoré uvažujú o mikrobióme ženského reprodukčného traktu ako o etiologickom faktore endometriózy. Predpokladá sa, že dysbióza sa môže podieľať na dysregulácii imunitného systému a zmene metabolizmu estrogénov. Štúdie ukazujú, že pacientky so zápalovými ochoreniami malej panvy, kde baktérie z pošvy ,,vycestovali“ do maternice, vajcovodov a vaječníkov, majú trikrát vyššie riziko vzniku endometriózy. To naznačuje, že ochorenie má čiastočne infekčnú etiológiu (4).
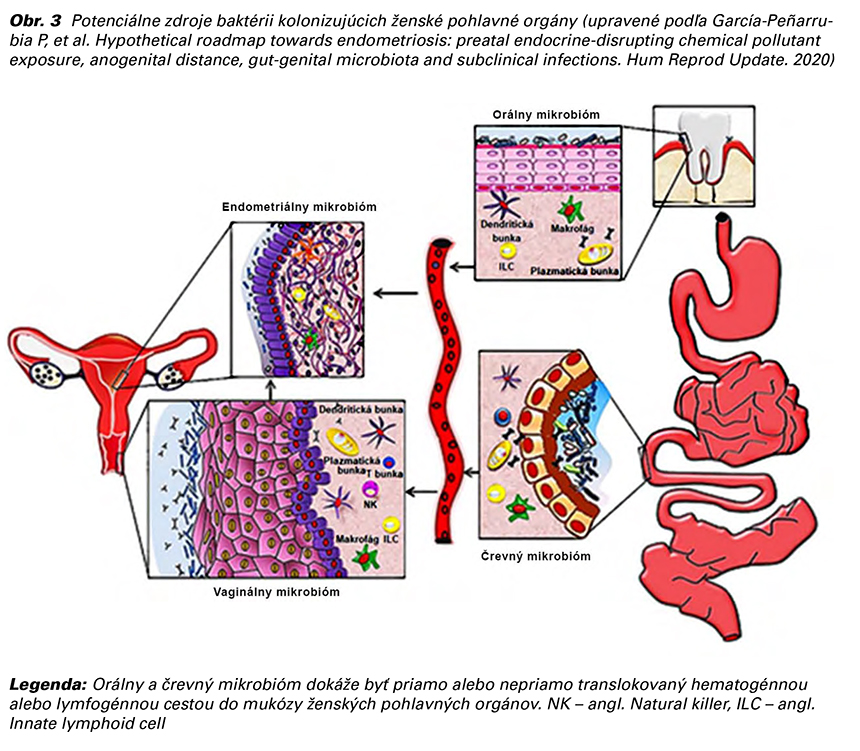
Nedávne štúdie sa snažili porovnať vaginálny, cervikálny a črevný mikrobióm u žien s endometriózou III. a IV. štádia so zdravými ženami (13). V cervikálnom mikrobióme u žien s endometriózou zistili zvýšený výskyt potenciálne patogénnych kmeňov Gardnerella, Streptococcus, Escherischia, Shigella a Ureaplazma. Črevný mikrobióm týchto žien obsahoval dominantne Shigellu a E. coli. Niekoľko ďalších štúdií zistilo, že endometriálny mikrobióm je značne zmenený u žien s ochoreniami maternice zahrňujúcich endometriózu. U žien s endometriózou bolo zvýšené zastúpenie Streptococcaceae, Moraxellaceae, Staphylococcaceae a Enterobacteriaceae, naopak znížené zastúpenie Lactobacillus spp. Ektopické lézie endometria mali vyššiu mikrobiálnu diverzitu ako eutopické endometrium (14). Doterajšie štúdie vo všeobecnosti potvrdili zvýšený výskyt baktérií spôsobujúcich bakteriálnu vaginózu a znížené množstvo Lactobacillus spp. v reprodukčnom trakte žien s endometriózou (13).
V štúdii, kde sa myšiam intraperitoneálne podávalo endometriálne tkanivo na vyvolanie endometriózy sa preukázalo, že po 42 dňoch pretrvávania endometrióznych ložísk dochádza k zmene črevnej mikroflóry. Inými slovami – progredujúca endometrióza mení zloženie mikrobiómu čriev. Pomer baktreriálnych kmeňov Firmicutes/Bacteroidetes je všeobecne akceptovaný ako znak dysbiózy. Medzi pozorovanými rozdielmi u myší s endometriózou a bez nej bol takmer dvojnásobný pomer Firmicutes/Bacteroidetes u endometriotických myší (7). Ďalšia štúdia potvrdzuje danú informáciu aj u opíc Maccacus rhesus. V porovnaní so zdravou skupinou mali opice s endometriózou nižšie zastúpenie Lactobacillus spp. a vyššie zastúpenie gram-negatívnych baktérií (15).
Na myšacom modeli autori štúdie zistili, že črevný mikrobióm podporuje vznik a rozvoj endometriózy. V tejto štúdii boli myšiam chirurgicky implantované endometriózne ložiská. Po čase im boli podávané antibiotiká, ktoré ložiská zmenšili. Následne boli podrobené transferu fekálneho mikrobiómu myší s aktívnou endometriózou. Endometriózne lézie opäť začali rásť a objavil sa u nich zápal (16).
Ďalší mechanizmus akým môže dysbióza čreva vyvolať endometriózu bol objasnený, keď pri výskume na opici Macacus rhesus s endometriózou bol pozorovaný vyšší výskyt črevných zápalov a črevnej dysbiózy (15). Črevný zápal je charakterizovaný prítomnosťou makrofágov, monocytov a sekréciou prozápalových cytokínov. Peritoneálny zápal možno pripísať vysokej koncentrácii cytokínov, čo je aj charakteristickým znakom endometriózy (17). Cytokíny majú schopnosť migrácie a je známe, že zohrávajú dôležitú úlohu pri sekrécii žalúdočnej kyseliny a črevnej motilite. Prítomnosťou cytokínov sa stáva vnútorné prostredie čreva menej priaznivé pre život Lactobacillov. Umožňuje tak rast gram-negatívnych baktérií. Týmto môžeme vysvetliť začarovaný kruh, kde dysbióza čreva prostredníctvom cytokínov môže spôsobiť vznik a progresiu endometriózy (15).
Okrem štúdií na animálnych modeloch sú publikované aj práce, ktoré zahŕňajú samotné pacientky s endometriózou. Shan et al. vo svojej štúdii podobne dokázali koreláciu medzi zápalovým procesom a črevným mikrobiómom pri vzniku endometriózy. Alterovaný črevný mikrobióm u pacientok s endometriózou ovplyvňuje RIG-I-like signálnu dráhu. Ak je táto signálna dráha aktivovaná, dochádza k iniciácii transkripcie určitých génov, a to najmä tých, ktoré sú asociované so zápalovým procesom. Uvažuje sa najmä o interleukíne 8, tumor nekrotizujúcom faktore α, či vaskulárnom a epidermálnom rastovom faktore. Táto štúdia bola realizovaná u 12 pacientok v III. a IV. štádiu endometriózy. Autori dokázali signifikantnú koreláciu medzi alterovaným črevným mikrobiómom a hodnotou estrogénu a pro-zápalových markerov. Nevýhodou je, samozrejme, malá vzorka pacientok (18).
Endometrióza je hormonálne závislé ochorenie. Väčšina symptómov sa manifestuje v reprodukčnom veku a odpovedá na hormonálnu liečbu (19). Estrogén stimuluje rast ektopického endometriálneho tkaniva, zvyšuje zápalovú aktivitu, alteruje estrogénne signálne dráhy. Ženy s endometriózou majú vyššie prozápalové a anti-apoptotické odpovede na estradiol kvôli zmenám v expresii jadrového estrogénového receptora. Ložiská endometriózy exprimujú vyššie hodnoty estrogénového receptora, prostredníctvom mediátorov zápalu vo zvýšenej miere aktivujú zápal a zvyšujú tak bunkovú adhéziu a proliferáciu (4).
Estradiol vzniká prostredníctvom enzýmu aromatázy, ktorý premieňa androgény na estrogény prostredníctvom steroidogénneho akútneho regulačného proteínu. Je to transportný proteín, reguluje prenos cholesterolu v mitochondriách, čo je potrebné na samotnú steroidogenézu. V ložiskách endometriózy je zvýšená expresia týchto látok, čo vedie k vzniku ochorenia. Normálne tkanivo endometria tieto enzýmy nemá a nie je schopné syntetizovať estrogén (19). Je známe, že metabolizmus estrogénu je regulovaný estrobolómom - kolekciou génov črevného mikrobiómu zapojených do jeho metabolizmu (20). Aktivita estrobolómov reguluje množstvo nadbytočného estrogénu, ktorý je vylúčený alebo reabsorbovaný do tela. V dôsledku nerovnováhy črevného mikrobiómu je táto činnosť narušená, nadbytok estrogénu sa zadržiava v tele, z čreva môže putovať do peritoneálneho prostredia prostredníctvom cirkulácie. To vedie k hyperestrogénnemu stavu, čo spôsobuje vznik a progresiu endometriózy (8).
Ako bolo spomenuté vyššie, kmeňové a progenitórové bunky kostnej drene sú schopné migrácie do ložiska endometriózy. Najnovšie štúdie dokazujú, že zloženie črevného mikrobiómu koreluje aj s množstvom kmeňových a progenitórových buniek v kostnej dreni, čím dokáže modulovať rast ektopického endometria (21).
V regulácii cirkulácie estrogénu hrá dôležitú úlohu taktiež metabolóm. Metabolóm zahŕňa všetky metabolity v danom prostredí, v tomto prípade v čreve. Je podstatne ovplyvnený črevnou mikrobiálnou aktivitou a obsahuje neuroaktívne metabolity, ktoré ovplyvňujú mozog a jeho signalizáciu. Ich prepojenie sa nazýva os črevo-mozog a spomínané neuroaktívne metabolity sa viažu na hormón uvoľňujúci gonádotropínové receptory (GnRH) stimulujúce produkciu luteinizačného hormónu (LH) a folikulostimulačného hormónu (FSH), ktoré následne stimulujú produkciu estrogénu (22).
Črevná mikroflóra sa podieľa na metabolizme estrogénov prostredníctvom lokálne pôsobiacej B-glukuronidázy, ktorá premieňa estrogén na jeho aktívnu formu, aby mohla byť naviazaná na estrogénový receptor. Pri črevnej dysbióze býva zvýšená koncentrácia B-glukuronidázy, čo zvyšuje množstvo estrogénu. Aktívny estrogén je následne transportovaný krvným obehom do distálnych mukóznych slizníc, ku ktorým patrí aj endometrium. Týmto spôsobom reguluje črevný mikrobióm estrogénovú rovnováhu v intestinálnych aj distálnych častiach. Pacientky s endometriózou majú vyšší počet črevných baktérií, ktoré produkujú B-glukuronidázu (4).
Švédske vedecké štúdie zistili súvislosti medzi systémovou zápalovou odpoveďou a endometriózou. Sérové koncentrácie niektorých zápalom podmienených proteínov sú pri endometrióze zvýšené. V experimente sa najviac zvýšila koncentrácia proteínov AXIN 1, ST1A1, pričom proteín CXCL mal tendenciu klesať. Koncentrácie týchto proteínov nemali súvis s anatomickou lokalizáciou endometriózy, ani s jej hormonálnou liečbou, korelovali však s prítomnými gastrointestinálnymi príznakmi. Cytoplazmatický proteín dôležitý pri regulácii apoptózy AXIN 1 bol objavený ako potenciálny nový biomarker endometriózy (23). Výrazné rozdiely v diverzite cervikálneho mikrobiómu u žien s endometriózou naznačujú, že vzorky získané z krčka maternice môžu byť použité na predpoveď možného vzniku endometriózy (24). Rovnako by mohli byť úspešne použité na predpovedanie štádia endometriózy aj profily vaginálnych mikrobiómov (25).
Liečba širokospektrálnymi antibiotikami preukázala účinnosť pri liečbe endometriózy na zvieracích modeloch. Nedávna štúdia zistila, že používanie širokospektrálnych antibiotík inhibuje rast endometrióznych ložísk. Liečba metronidazolom významne znížila zápal a zmenšila veľkosť ložísk (16). Nadmerné užívanie antibiotík však zvyšuje riziko antimikrobiálnej rezistencie. Antibiotiká sú účinné na elimináciu patogénov, avšak môžu spôsobiť trvalé narušenie črevného mikrobiómu (25). Použitie antibiotík na liečbu endometriózy si vyžaduje ešte rozsiahle výskumy. Efektívnym prístupom v liečbe endometriózy je podávanie probiotík. V randomizovaných placebom kontrolovaných štúdiách sa ukázalo, že perorálne podávanie probiotík zmenšuje bolesti u žien s endometriózou. Zmenšuje tiež endometriózne ložiská u myší tým, že zvyšuje koncentráciu NK buniek a IL-12. Dysbióza a endometriálny zápal vedú k narušeniu aktivity NK buniek. Probiotická liečba túto dysreguláciu zvrátila. Výskumy na potkanoch potvrdili, že liečba Lactobacilmi u zvierat zmenšila endometriózne ložiská (20).
Endometrióza sa ako chronické zápalové ochorenie ženského reprodukčného traktu vyskytuje v ambulanciách gynekológov čoraz častejšie. Súčasný životný štýl má negatívny dopad na zloženie črevného mikrobiómu, čo narúša aj iné systémy ľudského tela. Vedecké štúdie potvrdili súvislosť medzi dysbiózou čreva a endometriózou. Pri liečbe tohto ochorenia je preto na zváženie spolupráca medzi gynekológom a gastroenterológom. Správne stravovacie návyky, ktoré vedú k obnove a diverzite črevného mikrobiómu by mohli byť vhodnou prevenciou pred vznikom endometriózy, prípadne by mohli zabrániť jej progresii. Taktiež hormonálna liečba a úprava mikrobiómu by mohli priniesť adekvátne terapeutické výsledky.
Táto publikácia vznikla vďaka podpore v rámci Operačného programu Integrovaná infraštruktúra pre projekt: Nové možnosti manažmentu závažných ochorení v liečebno-preventívnej starostlivosti s ohľadom na bezpečnosť zdravotníckych profesionálov, kód projektu ITMS2014+: 313011AUA5, spolufinancovaný zo zdrojov Európskeho fondu regionálneho rozvoja.